01
引言
类器官工程是生物医学领域的前沿方向,通过构建模拟真实器官结构与功能的三维微型组织,为疾病建模、药物研发及再生医学提供了革命性平台。
近期,我们在国际权威期刊《Tissue Engineering: Part B》再次发表综述《Advances of Cell Printing Technology in Organoid Engineering》,系统梳理了细胞打印技术与类器官工程的深度融合,揭示了该领域的核心突破与未来趋势。

02
细胞打印技术的三大核心体系
综述重点解析了当前主流的三大细胞打印技术及其在类器官构建中的独特价值:
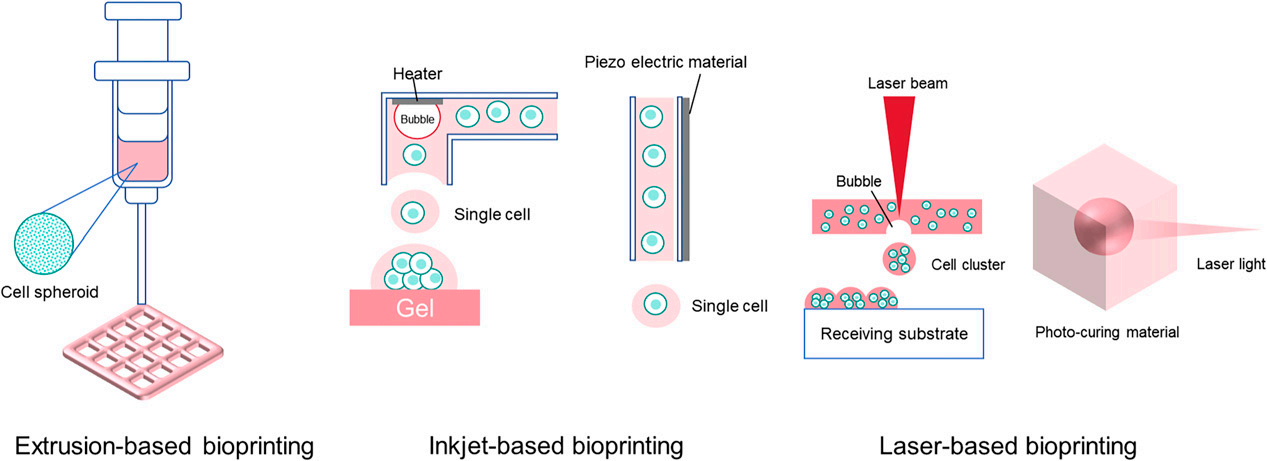
图丨根据其成型原理,细胞打印可分为三种类型:挤出式打印、喷墨式打印和激光式打印
1. 挤压式生物打印
该技术通过机械或气动压力驱动生物墨水沉积,是生物领域里最经典的3D打印技术,在此基础上,结合材料开发有产生了光固化打印、体式打印等等3D打印技术。其优势在于材料兼容性,比如利用不同材料打印管状组织如血管结构等,或以骨类器官为代表的强调刚性应力的器官体外再造;其局限性也非常明显,例如空间分辨率较低(约 100-500μm),比较适合构建较大的模型;蓝光固化过程中产生细胞活性损失(氧自由基等)或高粘度材料导致的高剪切力影响细胞活性等。除构建骨类器官以外,还曾报道利用该方法构建肝、肾脏、脑类器官等。
2. 喷墨式生物打印
基于热气泡或压电驱动原理可以实现pL级微液滴操控,由于液滴大小与细胞大小在同等量级,因而喷墨技术常常被认为可以实现单细胞级高通量操控,常用于单细胞分选或单克隆培养;如果使用喷墨技术构建类器官,在实现均一化类器官批量制备上更有优势,如构建体外小鼠肠道类器官高通量阵列用于药物筛选(见下图A到F);由于液滴小分辨率高(可以达到1200dpi以上)比较容易实现多细胞高精度的图像化打印,辅助用户构建具有复杂微环境(如免疫、成纤维等细胞)的类器官模型,在文献中用于构建多细胞共培养的三维肺纤维化模型。
此外, 由于液滴小可实现百微米级细胞高密度富集,从而提高类器官构建成功率,针对低密度样品或珍稀样本,该技术具有一定优势。
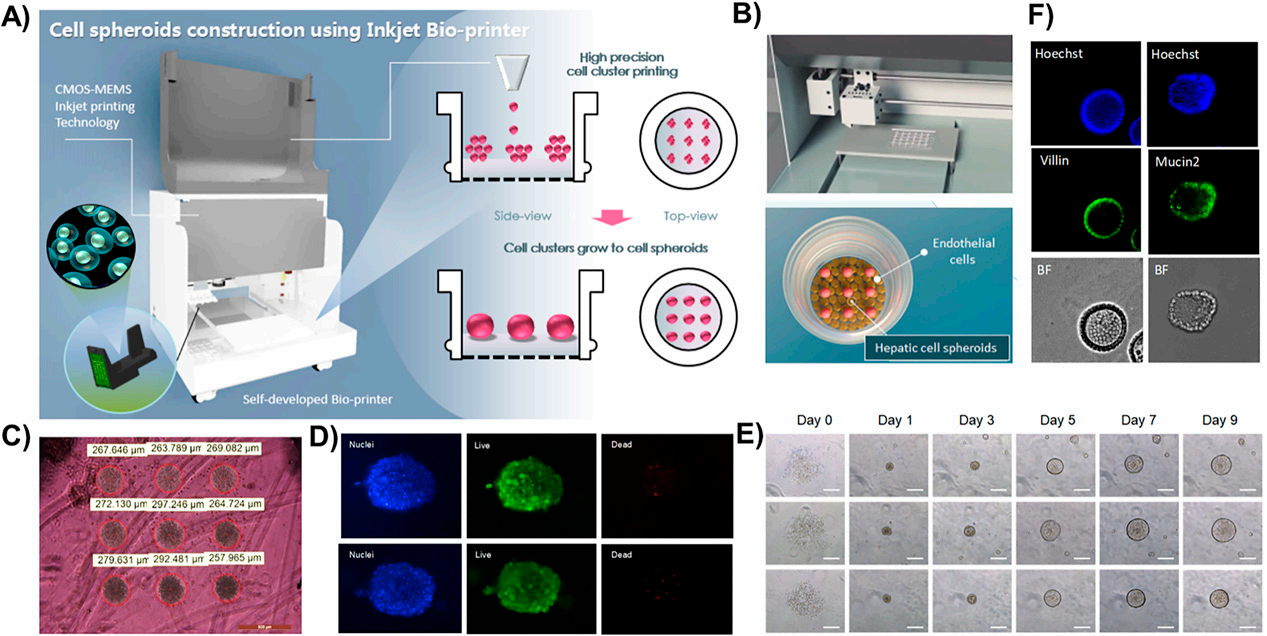
图丨喷墨打印技术在类器官组织工程中的应用。
(A,B)喷墨生物打印机生成的细胞球体和类器官。
(C)喷墨生物打印机打印的细胞簇阵列。
(D)喷墨打印的细胞球体的活/死细胞活力评估。
(E)来自小鼠肠道隐窝的细胞簇能够均匀生长成类器官。
(F)喷墨打印的小鼠肠道类器官中,包括Villin和Mucin2在内的肠道生物标志物的免疫荧光染色。
3. 激光辅助生物打印
利用激光能量诱导液滴喷射,实现亚细胞级精度(光斑直径 < 20μm),支持多种材料高分辨率沉积,但系统复杂、成本高。其非接触式打印使细胞存活率较高,适用于不同粘度生物墨水,却因人员操作门槛高和成本问题未广泛应用于类器官模型。应用上,可生成功能性肝脏类器官和胰腺球体阵列模型等。
03
类器官工程的多维度应用突破
综述系统总结了细胞打印技术在类器官工程中的创新应用:
疾病模型构建
结合挤压式打印与微流控技术,构建的脑胶质瘤类器官模型可模拟肿瘤微环境的异质性,其血管生成相关基因表达与临床样本吻合度达89%。该模型在抗癌药物筛选中显示出对靶向药物的响应差异,为个体化治疗提供新策略。
另外,采用液滴打印技术将前肠细胞与Matrigel混合后打印在柱状板上,形成多个形态功能一致的肝类器官,该模型具备白蛋白分泌和CYP3A4酶活性,在索拉非尼(sorafenib)与他莫昔芬(tamoxifen)处理下的反应与传统Matrigel圆顶培养一致。从而实现高通量人类肝脏类器官模型,生成结构一致的类器官,减少传统培养方法中常见的个体差异,提高实验可重复性。
3D生物打印技术为药物安全性研究提供更接近人体生理环境的模型,支持高通量筛选和个体化反应分析,有望大幅提升前期药物开发效率与准确性。
药物研发转化
将微流控系统与液滴式生物打印结合,能实现个别细胞的精准控制与排列。有利于高通量筛选与生物分析,提升生物模型的灵敏度与应用广度。3D生物打印作为补充工具,能自动、精准地沉积细胞或细胞基质材料,构建高通量的生物结构。例如: 利用喷墨打印技术所构建的微流控肝芯片模型(如下图MIMICup芯片所示) 通过动态共培养内皮细胞与肝细胞,成功复现中药肝毒性的病理特征,其预测价值显著优于传统二维模型。
该系统支持长达2周的连续灌流培养,可模拟临床长期给药场景,药物代谢酶活性与原代肝细胞一致性达92%。更有研究将3D生物打印与微传感器平台结合,实现了单个癌细胞类球的自动化沉积至带氧气感测电极的孔中,从而实时监测细胞呼吸速率与代谢活动。
总结以上研究成果可知微流控系统与3D生物打印的结合,构成了新一代高精度、自动化、可监测的器官芯片平台。可广泛应用于疾病建模、毒性评估、生理机制研究、个体化药物筛选等前沿领域。
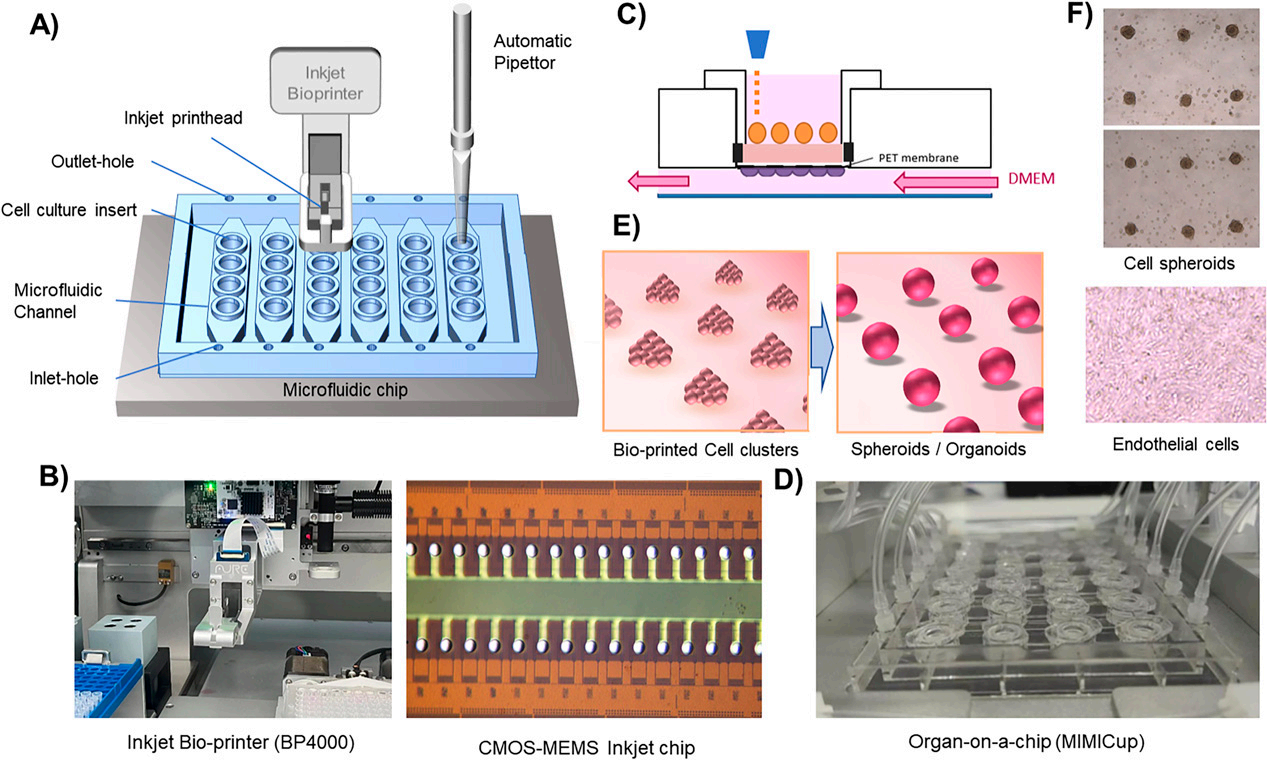
图丨3D生物打印与其他技术的整合。
(A)使用喷墨生物打印技术在器官芯片上播种细胞簇。
(B)BP4000生物打印机的喷墨生物打印头。
(C)组织芯片上的均匀大小的细胞球体/类器官。
(D)一个能够与生物打印技术结合的器官芯片平台(MIMICup)。
(E)生物打印的细胞簇生长成细胞球体。
(F)芯片上的细胞球体和内皮细胞。
04
技术挑战与未来方向
尽管细胞打印技术展现出巨大潜力,综述也指出其面临的核心挑战:
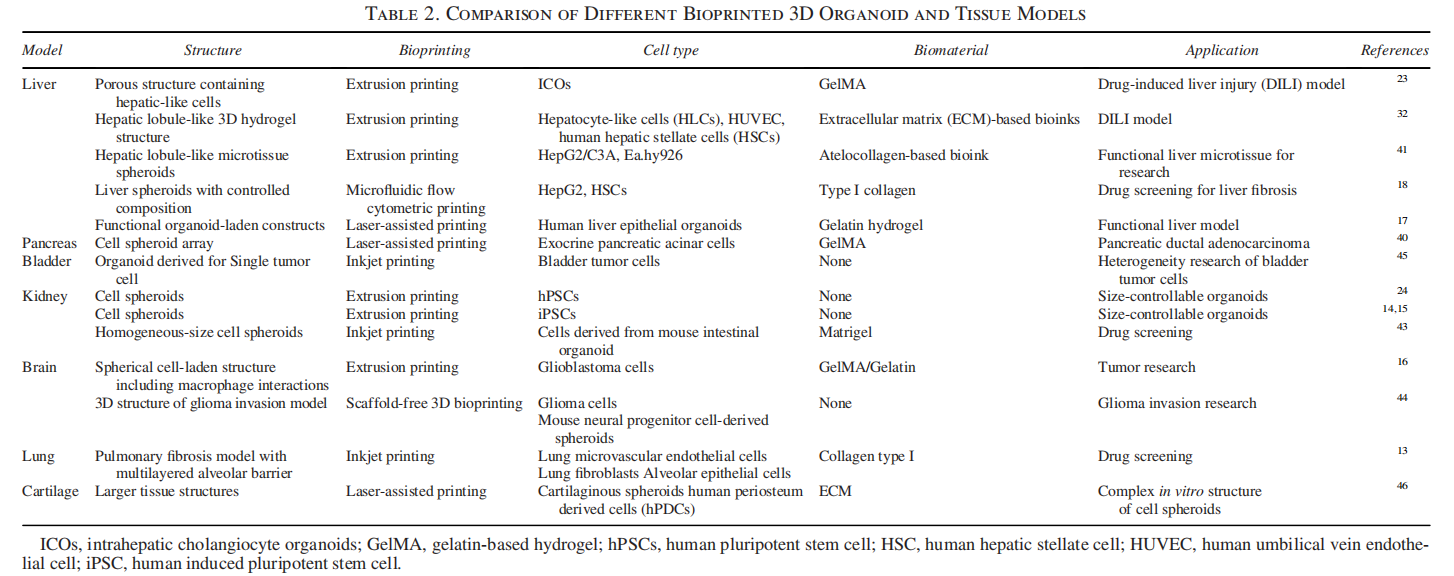
图丨不同生物打印的三维器官样和组织模型的比较
1. 生物材料瓶颈
现有生物墨水(如Matrigel)存在批次差异大、力学性能可调范围有限等问题。开发具有可降解性、仿生力学特性的新型复合水凝胶(如甲基丙烯酸酐化明胶/透明质酸复合体系)成为研究热点。
2. 标准化技术协议缺失
类器官构建的细胞密度、打印参数(如压力、温度)等缺乏统一标准,导致不同实验室间结果重复性差。建立基于机器学习的参数优化模型(如随机森林算法)被认为是解决该问题的关键路径。
3. 临床转化障碍
细胞打印类器官的长期体内稳定性、免疫原性及监管规范尚未明确。综述建议建立跨学科协作平台,整合材料科学、生物医学工程与临床专家资源,加速技术转化。
05
未来技术发展趋势
综述对细胞打印技术的未来方向做出前瞻性展望:
药物筛选模型打印
生物打印技术可实现高通量、重复性良好的类器官模型的批量构建,诸如利用生物打印技术所构建体外肝、肾、和癌症模型等,这些模型为临床研究者提供了更具有参考性并且可靠的药物筛选模型,并进一步改善了模型的精度和稳定性。
4D 生物打印
引入时间维度,开发可响应环境变化(如pH、温度)的智能类器官模型。例如,温敏性水凝胶构建的血管网络可在体内动态重构,为组织再生提供新范式。另外,构建符合空间时序的多细胞共培养体系也包含在这个概念内,如利用生物打印技术依照顺序先后在模型中沉积不同种类的细胞,形成在时间维度上仿真人体真实情况的共培养体系。
06
傲睿产品矩阵
覆盖 “构建 - 培养 - 检测” 的一体化类器官解决方案
傲睿在类器官与器官芯片领域构建了 “技术研发 - 产品落地 - 应用转化” 全链条的创新体系,其核心产品矩阵深度融合前沿技术突破,形成覆盖基础研究、药物开发、精准医疗的多元解决方案:
(1)自动化类器官构建系统BP4000

图丨自动化类器官构建系统BP4000
傲睿科技自主研发的自动化类器官构建系统 BP4000,基于液体数字化技术,能实现单细胞级精准操控,能有效提高批间一致性、缩短培养周期,为科研机构、药物研发提供标准化、高通量3D体外建模的解决方案。该系统集成光学辅助定位模块,可精准控制细胞接种位置,既可灵活调整模型尺寸,也可构建复杂微环境,提升3D体外建模仿生能力。系统创新性引入材料和细胞独立处理方案,采用水凝胶-培基界面培养,既简化后续免疫荧光染色流程,同时大幅提高光学检测效率。

图丨BP4000系统的工作原理
BP4000系统使用高通量并行控制的打印模式,配合高精度运动闭环控制,达到细胞喷射时间与细胞落点空间精确耦合的效果,实现在微米尺寸上高密度细胞接种以提高类器官构建成功率;同时,该系统配备光学成像识别单元并建立打印坐标系与视觉坐标系的实时空间配准,以满足二次建模及复杂微环境精确定位需求。
(2)类器官灌流系统MIMICup
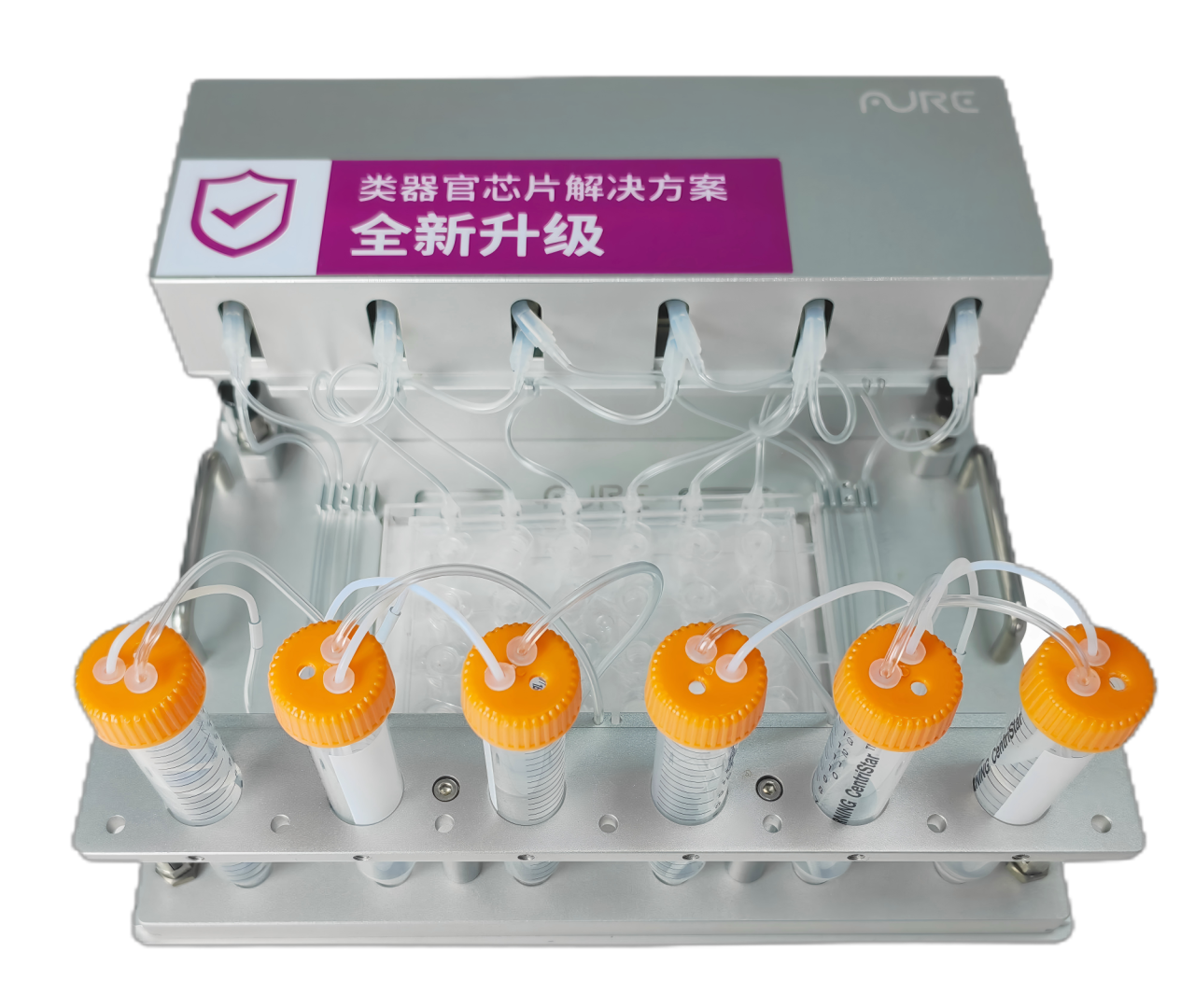
图丨类器官灌流系统MIMICup
MIMICup 微流控细胞培养板为带可插拔细胞培养小室的多细胞三维共培养支架,可构建物理力微环境,支持多种细胞垂直方向的分层三维共培养,其向上开口设计支持气液交界面(ALI)培养,便于结合3D生物打印技术,底部流道凹槽在小室安装后可形成密封流道,能为内皮细胞等提供剪切力微环境,所构建的类/器官芯片体外(invitro)组织模型与屏障模型更贴近体内状态,适用于化疗药的药敏/药效测试和新药研发前期筛选及科研应用等方向。
结构设计
MIMICup微流控细胞培养板采用特殊插拔式细胞培养小杯设计,便于操作与高通量应用,底部带有0.45um孔径高分子多孔膜与特殊密封层设计,前者提供多细胞三维立体共培养支架,后者在细胞培养版安装完成后可形成用于动态灌流培养的密封流道,本产品带有4个独立通道,共24个培养小室,可做复孔或多器官连通模型使用。
该系统通过微流控技术与模块化设计实现动态微环境精准控制,支持多细胞三维共培养、气液交界面建模及剪切力模拟,显著提升类器官培养功能性与稳定性。兼具高通量兼容及跨设备兼容适配能力,是连接类器官构建系统BP4000与功能检测的关键桥梁,为基础研究、新药研发及精准医疗提供了标准化、工程化的解决方案。
综述通过系统性梳理与深度分析,不仅明确了细胞打印技术在类器官工程中的核心地位 —— 从单细胞精准调控到复杂器官结构构建,从疾病模型解析到药物研发转化,其技术突破正持续打破传统研究的局限;更展现了该领域与工程化产品结合的创新潜力。
傲睿科技的自动化类器官构建系统BP4000 与类器官灌流系统MIMICup,正是这一趋势的具体实践:BP4000 以精准的液滴控制与标准化细胞球构建能力,夯实类器官制备的源头标准化基础;MIMICup 则通过动态微环境模拟与高通量设计,架起类器官功能验证与应用转化的桥梁。二者协同,形成“构建 - 培养 - 应用”的完整闭环,为基础研究与临床转化提供了工程化解决方案。
随着跨学科技术的深度融合与产品体系的持续迭代,细胞打印驱动的类器官工程必将加速从实验室走向临床,在精准医疗、再生医学等领域开辟更广阔的应用空间,成为生物医药创新的核心引擎。
更多内容可登录傲睿科技官网 www.aurefluidics.com 查看或下载原文
也可点击下方链接下载哦~












